康文医生的科普号
- 精选 “我有慢性肝病,能打新冠疫苗吗?”
“宝,我去打新冠疫苗了,打的什么苗,爱你的每一分每一秒”空军军医大学唐都医院传染病科康文“大夫,我有肝病,能打新冠疫苗吗?”“社区说慢性肝病吃着药不能打新冠疫苗”“有人说打疫苗要把药停了”……最近门诊有很多肝病患者都来咨询能否打新冠疫苗的问题。那到底哪些人能打,哪些不能打?打疫苗要不要停抗病毒药呢?打哪种疫苗呢? 慢性肝病(尤其是肝硬化)患者感染新冠病毒后,重症化和并发症发生率高。接种新冠疫苗是慢性肝病患者避免感染、降低感染后重症化的重要手段之一。首先,让我们来看看哪些肝病患者不能打。1. 肝衰竭者不能接种疫苗。2. 既往发生过疫苗严重过敏反应(如急性过敏反应、血管神经性水肿、呼吸困难等)者3. 患有未控制的癫痫和其他严重神经系统疾病(如横贯性脊髓炎、急性炎症性脱髓鞘性多发性神经病、脱髓鞘疾病等)者4. 正在发热者,或患急性疾病,或慢性疾病的急性发作期,或未控制的严重慢性病患者5. 妊娠期妇女。简单来说,就是肝病严重到已经住院的、正在怀孕的和严重过敏的三类人不能打。其他病情稳定、肝功基本正常的人均可以接种。接种疫苗期间,不停用原有治疗药物。“大夫,有打一针的,两针的和三针的,那应该打哪种疫苗呢?”我国已上市的新冠疫苗有三类,打一针的是腺病毒载体疫苗,两针的灭活疫苗,三针的重组亚单位疫苗。慢性肝炎的患者以上三类疫苗都是可以接种的,肝硬化患者建议首选接种灭活疫苗,也可以接种重组亚单位疫苗。明白了吗?一起来看看这些情况能不能打新冠疫苗呢?1. 乙肝小三阳,肝功正常,乙肝病毒定量未检出,从未接受过抗病毒治疗。答:能打,尽快接种。2. 慢性乙肝患者,长期口服恩替卡韦或替诺福韦抗病毒治疗,肝功正常,能打吗?答:能打,且不要停药。3. 乙肝肝硬化,吃着抗病毒药物,复查肝功正常,没有并发症,能打吗?答:能打,且不要停药。建议首先接种灭活疫苗,也可考虑重组亚单位疫苗。4. 乙肝大三阳,肝功不正常,病毒量高,能打吗?答:暂缓接种,先抗病毒治疗,等病情稳定了、肝功正常了再接种。5. 肝硬化,有明显乏力、恶心、腹胀等症状,有黄疸、腹水,能打吗?答:先住院吧,坚决不能打,等出院了再说。6. 肝病患者,突然吐血、便血了,能打吗?答:先去急诊科抢救呀,疫苗就别打了。7. 我父亲有肝癌,做了介入手术,现在病情控制的还好,能打疫苗吗?答:癌症患者是新冠的高危人群。对此类人群疫苗接种的数据尚缺乏,接种后的免疫反应及保护效果可能会降低。如果病情稳定,建议接种打两针的灭活疫苗和打三针的重组亚单位疫苗。8. 乙肝女性,最近准备备孕,能打疫苗吗? 男方能打吗?答:双方都可以打。对于有备孕计划的女性,不必仅因接种新冠病毒疫苗而延迟怀孕计划。如果在接种后怀孕或在未知怀孕的情况下接种了疫苗,不推荐因接种新冠病毒疫苗而终止妊娠,建议做好孕期检查和随访。9. 我有乙肝,要做试管婴儿,能打疫苗吗?答:对人工辅助生殖方面没有相关研究,但参考推荐意见,备孕阶段可以接种,已经受孕了就暂缓接种。10. 乙肝女性,已经怀孕了,能打吗?答:妊娠期妇女不建议接种新冠疫苗。先去做乙肝母婴阻断吧。11. 丙肝抗体阳性,既往曾使用过抗病毒治疗,已停药,多次复查丙肝病毒定量均未检出,能打吗。答:目前丙肝已经痊愈,可以打。12. 丙肝患者,正在吃抗病毒药,能打吗?答:肝功正常时可以打,打疫苗时不要停药。也可等治疗结束了再打,毕竟就只吃三个月的药。13. 我有肝病,但是我发烧了,能打吗?答:暂缓接种,等恢复正常了再接种。14. 自身免疫性肝病,吃着激素和熊去氧胆酸胶囊,能打吗?答:病情控制稳定是可以正常打的,不用停药。15. 最近我要注射乙肝疫苗、出血热疫苗等,能打新冠疫苗吗?答:不建议与其他疫苗同时接种。与其他疫苗需分开接种,且接种时间间隔至少两周,以尽量减少非预期的相互作用,也便于观察接种后的反应。16. 我比较胖,检查了说我有脂肪肝,转氨酶轻度异常,能打新冠疫苗吗?答:胖也不是错,既往的临床试验中也纳入了脂肪肝患者,证实是安全有效的,可以接种,接种流程和其他人一样。 17. 我喝了几场酒,查出来酒精肝,转氨酶严重不正常,能打吗?答:肝炎急性活动期是不建议打疫苗的,还是先戒了酒,保肝治疗待好转后再行接种。好了,大家安心的接种疫苗吧,还有不明白的再来感染科咨询专科医生,万不可自行停药哦。参考文献:1. 中华医学会感染病学分会, 中华医学会风湿病学分会. 特殊人群(慢性肝病、结核病和风湿免疫病患者)新型冠状病毒疫苗接种专家建议 [J] . 中华传染病杂志, 2021, 39(0) : E002-E002. 2. 国家卫生健康委员会.新冠病毒疫苗接种技术指南(第一版)[EB/OL].(2021-03-29) [2021-05-07]. https://www.gov.cn/xinwen/2021-03/29/content_5596577.htm.3. Fix OK, Blumberg EA, Chang KM, et al. AASLD expert panel consensus statement: Vaccines to prevent COVID-19 infection in patients with liver disease[J/OL].Hepatology, 2021:10.1002/hep.31751(2021-02-12) [2021-05-07]. https://doi.org/10.1002/hep.31751.
康文 副主任医师 空军军医大学唐都医院 传染病科1.1万人已读 - 精选 2020艾滋病抗病毒治疗进展及新药
本幻灯总结了国内及国际指南中关于HIV抗病毒治疗时机、抗病毒方案的推荐更新,以及新的抗HIV治疗药物靶点和进展。适合专业人士阅读
康文 副主任医师 空军军医大学唐都医院 传染病科4人已购买 - 直播回放 口腔念珠菌病治疗知多少
直播时间:2022年04月28日19:31主讲人:康文副主任医师空军军医大学唐都医院传染病科
 康文 副主任医师 空军军医大学唐都医院 传染病科327人已读
康文 副主任医师 空军军医大学唐都医院 传染病科327人已读 - 直播回放 拿什么拯救你,HIV感染者的精神健康
直播时间:2022年03月19日09:58主讲人:康文副主任医师空军军医大学唐都医院传染病科
 康文 副主任医师 空军军医大学唐都医院 传染病科502人已读
康文 副主任医师 空军军医大学唐都医院 传染病科502人已读 - 医学科普 艾滋病的“后悔药”
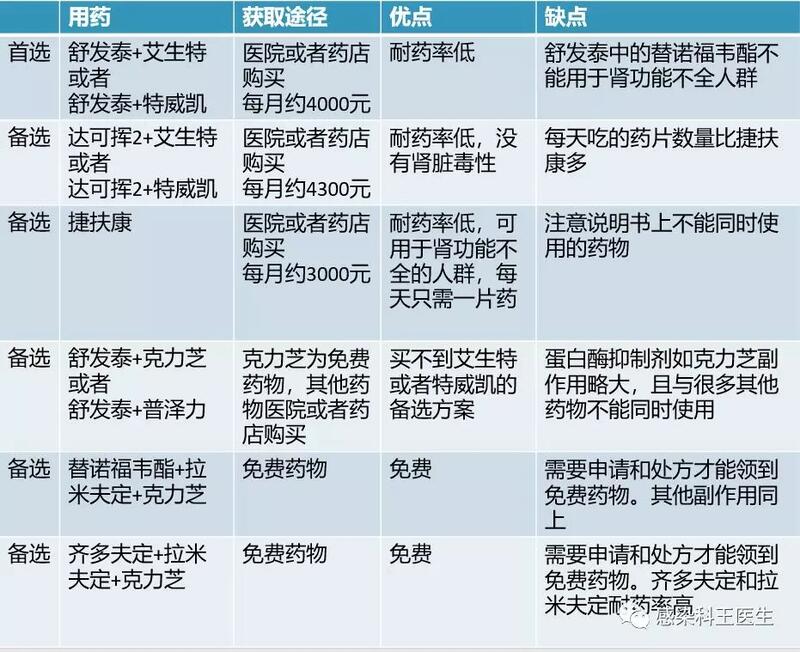
1.艾滋病能否治愈?治疗难度如何? 艾滋病病毒是一种逆转录病毒,入侵人体T细胞后,能借助逆转录酶将自身的RNA逆转录为双链DNA,再借助整合酶将DNA整合到人体细胞的基因组中,这样一来艾滋病病毒就彻底的和人的免疫细胞融为一体了,同时,一部分受感染的细胞还能潜伏起来,形成病毒储存库,伺机繁殖。这就是艾滋病难以彻底治愈的原因。病毒的RNA就如同小草,DNA如同草根,我们的抗病毒药物只能抑制RNA,但对DNA无效,因此,目前的抗病毒治疗不能彻底治愈艾滋病,只能抑制病毒,需要终身用药,一旦停药很快就会导致病毒反弹、免疫系统破坏加剧。也就是野火烧不尽,春风吹又生。20多年前,最初的抗病毒鸡尾酒疗法需要一天吃十几片药,而现在已经有了复方单片药,一天只需要吃一片就可以控制病毒复制,恢复免疫功能,而且未来抗病毒药越来越先进、方便,长效,很快就会有一个月打一针甚至半年打一针的长效药。 2.什么是艾滋病暴露后预防,能否阻断艾滋发生 艾滋病暴露后预防是对未感染艾滋病的人,在暴露于高感染风险后,通过服用特定的抗艾滋病药物,来阻断艾滋病病毒感染风险的方法。按医嘱规范的进行暴露后预防,可以成功阻断艾滋病感染。 3.发生高危性行为后该怎么办? 发生无保护的阴道性交或肛交,应在立即进行暴露后预防,也就是吃上“后悔药”。暴露后预防的方案很多,主要是以整合酶抑制剂为核心的三联药物组合方案,可用的方案有:替诺福韦加恩曲他滨,联合多替拉韦,也就是舒发泰(舒发泰是替诺福韦加恩曲他滨二联复方药)+特威凯,也可用达可挥(达可挥是丙酚替诺福韦+恩曲他滨二联复方药)+特威凯,或者必妥维、捷扶康(二者都是复方单片药)等。暴露后预防启动时间越快越好,尽可能在2小时内服药,最好在24小时内服药,最长不超过72小时,并且按疗程服完28天,这样几乎可百分百阻断成功,超过72小时基本上无效。同时,在服药前、服药后和停药3个月时分别进行一次HIV抗体、乙肝五项检测以评估阻断效果。如果停药后3月复查HIV抗体阴性,就代表阻断成功。
康文 副主任医师 空军军医大学唐都医院 传染病科690人已读 - 医学科普 乙肝能办健康证吗?
“乙肝能办理健康证吗?”对于这个问题,很多人存在困惑。首先我们要将“健康证”和“健康”区分开来,“健康证”≠“健康”。“健康证”制度是法律的要求。我国于2009年6月1日正式实施新的《中华人民共和国食品安全法》(2021年4月29日第二次修订),7月20日又出台《实施条例》。1987年4月1日国务院发布《公共场所卫生管理条例》(2019年4月23日第二次修订)。根据《食品安全法》第四十五条之规定:“食品生产经营者应当建立并执行从业人员健康管理制度。患有国务院卫生行政部门规定的有碍食品安全疾病的人员,不得从事接触直接入口食品的工作。从事接触直接入口食品工作的食品生产经营人员应当每年进行健康检查,取得健康证明后方可上岗工作。”第一百二十六条规定:有“食品生产经营者安排未取得健康证明或者患有国务院卫生行政部门规定的有碍食品安全疾病的人员从事接触直接入口食品的工作”情形的,由“县级以上人民政府食品药品监督管理部门”给予处罚。根据上述法律规定,食品生产经营者应当对从业人员开展健康管理,其管理情况由食品药品监督管理部门进行监管。根据《公共场所卫生管理条例》第七条之规定:“公共场所直接为顾客服务的人员,持有“健康合格证”方能从事本职工作。患有痢疾、伤寒、病毒性肝炎、活动期肺结核、化脓性或者渗出性皮肤病以及其他有碍公共卫生的疾病的,治愈前不得从事直接为顾客服务的工作。”可见,根据《食品安全法》、《公共场所卫生管理条例》等法规,从事食品生产经营,公共场所服务,化妆品、一次性医疗卫生用品等专业生产,有毒、有害、放射性作业,幼托机构保育这五大行业的相关人员必须拥有健康证。那么,哪些疾病是“卫生行政部门规定的有碍食品安全疾病”呢?为落实《食品安全法》、《传染病防治法》,2015年国家卫生计生委牵头组织制定《有碍食品安全的疾病目录》,为监管部门和食品生产经营者对从业人员进行健康管理提供依据。目录根据实际情况对部分病种进行了细化,如痢疾、病毒性肝炎,修改为细菌性和阿米巴性痢疾、病毒性肝炎(甲型、戊型)。《目录》中具体包含霍乱、细菌性和阿米巴性痢疾、伤寒和副伤寒、病毒性肝炎(甲型、戊型)、活动性肺结核、化脓性或者渗出性皮肤病6类疾病。(《有碍食品安全的疾病目录》解读_部门_中国政府网 (www.gov.cn))艾滋病、乙肝不在列!《目录》中所列疾病首先要具备可以经食物传播的特点,而艾滋病和乙肝虽然都属于危害较大的传染性疾病,其传播途径并不包括经食物传播。艾滋病的传播途径主要有:性接触传播、血液传播和母婴传播;乙肝的传播途径主要有:血液传播、母婴传播和性接触传播。日常工作或生活接触,如握手、拥抱、共同就餐等无血液暴露的行为,不会传播上述疾病。因此,根据国家法规,有乙肝的患者是可以办理健康证、从事食品行业的。虽然乙肝患者可以办理健康证,并不是代表乙肝患者就是健康的,乙肝患者病情不稳定很容易恶化,乙肝患者可能出现肝炎活动,定期监测和及时的抗病毒治疗是控制病情进展的关键措施。
康文 副主任医师 空军军医大学唐都医院 传染病科1042人已读 - 医学科普 【共识】阻断乙型肝炎病毒母婴传播临床管理流程(2021年)
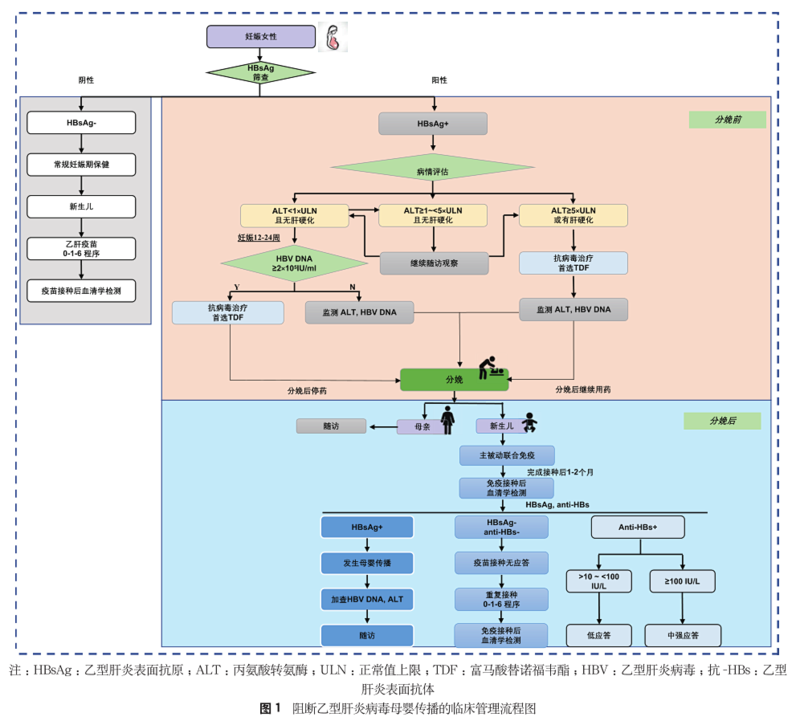
转自中华肝脏病杂志2016 年 5 月,世界卫生大会通过了《全球卫生部门病毒性肝炎战略(2016-2021)》,这一战略提出至 2030 年消除病毒性肝炎公共卫生威胁的目标(包括至 2030 年,在 2015 年数据的基础上将新发病毒性肝炎感染率降低 90%,并将病毒性肝炎引起的病死率减少 65%)[1] 。其中,消除乙型肝炎(以下简称乙肝)对公共卫生威胁需要将 5 岁儿童的乙型肝炎病毒(HBV)感染率降至 0.1%。母婴传播是 HBV 的重要传播途径,阻断 HBV 母婴传播是消除乙肝的关键,加强慢性 HBV 感染孕妇及其所分娩婴儿的规范化管理是切断 HBV 母婴传播的有效措施。近年来,国内外实施的消除病毒性肝炎策略为消除 HBV 母婴传播提供了有利时机。为进一步规范我国 HBV 母婴传播阻断的临床管理,中国肝炎防治基金会于 2017 年组织专家编写并发表了《乙型肝炎母婴阻断临床管理流程》 [2 - 3] 。该流程已在阻断 HBV 母婴传播的临床实践中得到了广泛应用,对预防 HBV 母婴传播的工作起到了积极的促进作用。近年来,阻断 HBV 母婴传播成为公共卫生领域的热点,围绕这一热点的相关研究取得了令人瞩目的进展。现参照近期国内外发表的预防乙肝母婴传播的指南或共识和最新研究成果 [4 - 15] ,对第 1 版《乙型肝炎母婴阻断临床管理流程》进行更新,以帮助临床医师更新观念,并为阻断 HBV 母婴传播提供规范的临床管理。 一、感染 HBV 孕妇的筛查我国是乙肝的中高流行区,一般人群中 HBsAg 阳性率约为 6.1% [16] ,孕产妇中 HBsAg 阳性率约为 6.3% [17] 。在孕妇中普遍筛查 HBV 感染的血清学标志物是实施 HBV 母婴阻断的第 1 个环节。我国预防艾滋病、梅毒和乙肝母婴传播项目要求,所有妊娠早期孕妇均应筛查艾滋病、梅毒和乙肝 [18] 。筛查 HBV 血清学标志物应包括 HBsAg 和抗 - HBs。若孕妇 HBsAg 阴性,通常表明无 HBV 感染,给予常规妊娠期保健服务,并了解其丈夫有无 HBV 感染 ;若孕妇 HBsAg 阳性,表明存在 HBV 感染,需详细询问病史及家族史,并按管理流程评估 HBV 感染相关情况。由于乙肝存在家庭聚集性,建议其家庭成员筛查乙肝。 二、HBV 感染的病情评估及治疗HBsAg 阳 性 孕 妇 需 检 测 HBeAg、 抗 - HBe、HBV DNA 水平、肝功能生物化学指标和上腹部超声检查,以判断其是否出现肝炎活动及进行纤维化分期,需特别关注是否存在肝硬化。 1. 若 HBV DNA 阳性,出现 ALT 显著异常,≥ 5×正常值上限(upper limit of normal,ULN),排除导致 ALT 升高的其他相关因素(如药物和脂肪肝等),或诊断为肝硬化者,经感染病或肝病专科医师评估及患者知情同意后,建议给予替诺福韦酯(tenofovir disoproxil fumarate,TDF)抗病毒治疗。 2. 若 HBV DNA 阳性,ALT 为(1 ~ < 5)×ULN,且总胆红素(TBil)< 2×ULN 时,可继续观察,如果观察期间ALT≥5×ULN,或TBil≥2×ULN,则按上述“二、1.”部分处理;如果 ALT < 1×ULN,则按“二、3.”部分处理;如果随访至妊娠 24 周 ALT 仍为(1 ~ < 5)×ULN,经患者知情同意后,给予 TDF 进行抗病毒治疗。 3. 若 HBV DNA 阳性,ALT 正常,无肝硬化表现,可以暂不治疗,继续观察肝功能情况。在随访期间,如果出现 ALT 持续升高(ALT ≥ 1×ULN),则根据 ALT 水平按“二、1.”或“二、2.”部分处理,注意 TBil 和凝血酶原活动度(PTA)的检查结果,用于判断肝脏损伤的严重程度。 4. 若 HBV DNA 低于检测下限,表明患者可能处于非活动期,建议于妊娠 24 周复查 HBV DNA,若仍低于检测下限,则无需干预。 对于出现乙肝活动而需要进行抗病毒治疗的孕妇,治疗药物首选 TDF,如果患者存在骨质疏松、肾损伤或肾损伤的危险因素,可选用富马酸丙酚替诺福韦(tenofovir alafenamide fumarate,TAF)治疗。 三、阻断 HBV 母婴传播的抗病毒治疗对于高 HBV 载量的孕妇,在妊娠晚期进行抗病毒治疗,结合新生儿乙肝疫苗及乙型肝炎免疫球蛋白(hepatitis B immunoglobulin,HBIG)的接种,能够进一步降低 HBV 母婴传播发生率,并且未增加胎儿的不良妊娠结局 [9 - 11] 。因此,妊娠期抗病毒治疗阻断 HBV 母婴传播已被广泛接受并应用于临床实践中,对消除 HBV 母婴传播起到了积极的作用 [15] 。 经病情评估后肝功能正常的未服用抗病毒药物的孕妇,在妊娠中期检测 HBV DNA 水平(推荐采用高灵敏试剂检测),根据 HBV DNA 水平,决定是否需要进行抗病毒治疗以阻断 HBV 母婴传播。如果无条件检测 HBV DNA 定量,可以 HBeAg 作为其替代指标,HBeAg 阳性者给予抗病毒治疗 [6] 。 1. 若孕妇 HBV DNA ≥ 2×10? IU/ml,经知情同意后,可于妊娠 28 周给予 TDF 进行抗病毒治疗。如果孕妇存在骨质疏松、肾损伤或导致肾损伤的高危因素,或消化道症状严重,可以选择 TAF 或替比夫定(telbivudine)。分娩前应复查 HBV DNA,以了解抗病毒治疗效果及 HBV 母婴传播的风险。 TAF 在我国被批准上市后,在母婴传播阻断的临床研究和临床实践中得到了初步应用。现有数据表明,TAF 用于妊娠期 HBV 母婴传播阻断的效果和安全性良好 [13 - 14] 。TAF 有望成为妊娠期抗病毒阻断 HBV 母婴传播的新选择。 2. 若孕妇 HBV DNA < 2×10? IU/ml,发生 HBV 母婴传播的风险低,一般对其新生儿给予乙肝疫苗 +HBIG 免疫即可预防,不需要抗病毒治疗。 3. 对于超过妊娠 28 周首次就诊的孕妇,若 HBV DNA ≥ 2×10? IU/ml,仍建议尽早给予抗病毒治疗。 四,分娩及新生儿的护理1. 分娩方式 :关于分娩方式与 HBV 母婴传播的关系,现有研究结果不一致。虽然有研究显示,剖宫产可以减少高病毒载量孕妇所生婴儿的 HBV 感染发生率 [19 - 20] ;然而荟萃分析的结果表明,分娩方式与 HBV 母婴传播风险没有确切关系 [21] ,剖宫产并未降低 HBV 母婴传播的发生率,故不建议根据 HBV DNA 水平或 HBeAg 状态选择分娩方式,应根据产科指征决定分娩方式。 2. 新生儿护理 :新生儿出生后立即移至复苏台,离开母血污染的环境 ;彻底清除体表的血液、黏液和羊水 ;处理脐带前,需再次清理、擦净脐带表面血液等污染物,按操作规程安全断脐。 五,停药的时机妊娠期服用抗病毒药物的母亲的停药时机取决于妊娠期抗病毒治疗的目的 :①以阻断 HBV 母婴传播为目的而服用抗病毒药物的孕妇,分娩后检测 HBsAg 和 a定量,如果 HBsAg 和(或)HBeAg 水平显著下降,提示抗病毒治疗效果良好,可继续抗病毒治疗。如果 HBsAg 和(或)HBeAg 水平下降不明显,产后立即停药。②以治疗乙肝为目的而服用抗病毒药物的孕妇,产后不能停药,应长期抗病毒治疗。 六,婴儿的免疫新生儿免疫接种是阻断 HBV 母婴传播的最重要措施,对于母亲是 HBsAg 阳性孕妇的新生儿,首剂乙肝疫苗和 HBIG 的接种时机非常关键。新生儿出生后 12 h 内应尽快完成乙肝疫苗和 HBIG 的联合免疫 [2,22] ;HBsAg 阴性母亲的新生儿应于产后 12 h 内尽快完成首剂乙肝疫苗接种。 1. 常规疫苗接种 :在新生儿大腿前部外侧肌肉或上臂三角肌内接种重组酵母乙肝疫苗 10 μg/0.5 ml,同时在对侧相应部位注射 HBIG 100 IU,在其 1 月龄和 6 月龄时分别接种相同剂量的第 2 和第 3 针乙肝疫苗。 2. 正常产新生儿的免疫接种 :①对于 HBsAg 阳性母亲的新生儿,于出生 12 h 内接种重组酵母乙肝疫苗 10 μg/0.5 ml + HBIG 100 IU,并于 1 和 6 月龄各注射 1 针重组酵母乙肝疫苗 10 μg/0.5 ml ;②对于 HBsAg 不详母亲的新生儿,则按母亲 HBsAg 阳性处理,即于出生 12 h 内接种重组酵母乙肝疫苗 10 μg/0.5 ml + HBIG 100 IU,同时尽快检测母亲 HBsAg,明确母亲是否为 HBsAg 阳性后,按规范及时为婴儿接种乙肝疫苗 ;③对于 HBsAg 阴性母亲的新生儿,于出生 12 h 内接种重组酵母乙肝疫苗 10 μg/0.5 ml,并于 1 和 6 月龄各注射 1 针重组酵母乙肝疫苗 10 μg/0.5 ml。 3. 低体质量儿(< 2 000 g)或早产儿(< 妊娠 37 周)的免疫接种 :①对于 HBsAg 阳性母亲的低体质量儿或早产儿,于出生 12 h 内尽快完成联合免疫,即接种重组酵母乙肝疫苗 10 μg/0.5 ml+HBIG 100 IU,并于 1、2 和 7 月龄各注射 1 针重组酵母乙肝疫苗 10 μg/0.5 ml ;②对于 HBsAg 不详母亲的低体质量儿或早产儿,于出生 12 h 内尽快完成联合免疫,即接种重组酵母乙肝疫苗 10 μg/0.5 ml+HBIG 100 IU,同时尽快检测母亲 HBsAg,明确母亲是否为 HBsAg 阳性后,按规范及时为婴儿接种乙肝疫苗。③对于 HBsAg 阴性母亲的低体质量儿或早产儿,最好于出生 12 h 内接种首针重组酵母乙肝疫苗 10 μg/0.5 ml,并于 1、2 和 7 月龄各注射 1 针重组酵母乙肝疫苗 10 μg/0.5 ml ;也可在出院时或 1 月龄时接种重组酵母乙肝疫苗 10 μg/0.5 ml,并在 2 和 7 月龄各接种 1 针乙肝疫苗(10 μg/0.5 ml)。 4. 危重症新生儿的免疫接种 :新生儿如为极低出生体质量儿(< 1 500 g)、或有严重出生缺陷、重度窒息、呼吸窘迫综合征等,应在其生命体征平稳后尽早接种 [ 参照低体质量儿(< 2 000 g)或早产儿(< 妊娠 37 周)的免疫接种 ]。 5. 疫苗延迟接种的处理 :为保证婴儿乙肝免疫接种的效果,建议严格按 0-1-6 免疫程序接种,特别是 HBsAg 阳性母亲的新生儿,尽量不延期接种。如婴儿有特殊情况,不能如期接种第 2 针乙肝疫苗,可延迟接种,但最长不能超过 3 个月,第 3 针疫苗仍可在 6 月龄时注射。 七,母乳喂养母乳喂养并未增加婴儿的 HBV 感染率 [23 - 24] ,感染 HBV 母亲分娩后可以哺乳。没有必要检测乳汁中的 HBsAg 和(或)HBV DNA。 1. 母亲未服用抗病毒药物的新生儿,在接受规范的联合免疫后可以进行母乳喂养 [2 - 8] ,母乳喂养并未增加 HBV 母婴传播的发生率。如母乳喂养期间母亲出现乙肝活动,可参照《慢性乙型肝炎防治指南(2019 年版)》 [4] 中慢性乙型肝炎患者的治疗原则给予抗病毒治疗,如果接受 TDF 治疗,可以母乳喂养。 2. 以阻断 HBV 母婴传播为目的而服用抗病毒药物的孕妇,分娩后停药,婴儿接受联合免疫之后,可以母乳喂养。 3. 以治疗乙肝为目的而服用抗病毒药物的孕妇,分娩后应继续用药,如果服用 TDF 治疗,因 TDF 在乳汁中的药物含量很少 [25] ,婴儿可以接受母乳喂养。 八,母亲产后的随访HBV 感染母亲产后可能出现 ALT 升高。研究表明,产后 24 周内约有 28% 的 HBV 感染母亲出现肝功能异常,孕妇 HBV DNA 高载量是产后肝功能异常的危险因素 [26] 。 1. 产后继续服用抗病毒药物者,按慢性乙型肝炎患者的随访方案进行随访,分娩后 1 年内每 3 个月复查肝功能、HBV DNA,每 6 个月复查乙肝血清学标志物、甲胎蛋白、上腹部超声和肝脏瞬时弹性成像。 2. 产后停药者及未服用抗病毒药物者,产后 6 ~ 8 周复查肝功能生物化学指标和 HBV DNA。如果肝功能正常,分娩后每 3 个月复查肝功能、HBV DNA ;如果肝功能异常且符合抗病毒治疗指征,应启动抗病毒治疗。 九,婴儿免疫接种后的血清学检测对于 HBsAg 阳性母亲的婴儿,在完成乙肝全程免疫接种 1 ~ 2 个月后,需抽取静脉血检测 HBV 血清学标志物,至少包括 HBsAg 和抗 - HBs,建议采用定量检测方法。如 HBsAg 阳性,还需进一步检测 HBV DNA 水平和肝功能生物化学指标,以后每 6 个月随访 1 次,复查肝功能生物化学指标和病毒学指标。 十,婴儿乙型肝炎免疫接种的效果评价1. 免疫接种成功 :婴儿完成乙肝全程免疫接种 1 个月后随访,如果 HBsAg 阴性,但抗 - HBs 阳性(抗 - HBs ≥ 10 mIU/ml),表明免疫接种成功。如果抗 - HBs < 100 mIU/ml,为低应答 ;如果抗 - HBs ≥ 100 mIU/ml,为中强应答。无论低应答还是中强应答,均无必要再次接种乙肝疫苗。 2. 免疫接种无应答 :婴儿完成乙肝全程免疫接种后血清学检测结果显示,HBsAg 阴性和抗 - HBs < 10 mIU/ml。无论抗 - HBe 及抗 - HBc 阳性与否,都需按 0 - 1 - 6 程序重复免疫接种,仍使用重组酵母乙肝疫苗 10 μg/0.5 ml。完成重复接种后 1 个月,再次检测 HBsAg 和抗 - HBs,了解免疫应答和 HBV 感染情况。 3. 免疫接种失败,发生 HBV 母婴传播 :婴儿完成乙肝疫苗全程免疫接种 1 个月后随访,HBsAg 阳性,伴或不伴 HBeAg 阳性。发生 HBV 母婴传播的婴儿,还需检测 HBV DNA 和肝功能,并按慢性 HBV 感染者进行随访。如果出现肝炎活动,应及时进行抗病毒治疗,可以选择 α 干扰素、恩替卡韦或 TDF 治疗儿童乙肝患者。 将上述 10 个环节的要点总结为管理流程图(图 1),便于在临床实践中参考。 十一,待解决的问题1. 抗 HBV 新药 TAF 是否可用于 HBV 母婴传播阻断:我国已于 2018 年批准 TAF 用于治疗慢性乙型肝炎。作为 TDF 的改进版,TAF 降低了肾损伤、骨密度降低等不良事件的发生率,目前已被美国肝病学会、欧洲肝病学会、中华医学会感染病学分会和肝病学分会制订的乙肝防治指南推荐为抗 HBV 的一线用药。 既然 TAF 比 TDF 安全,是否可以用于妊娠期阻断 HBV 母婴传播?国内外学者已对这一问题开展了临床研究,并且发表了初步的研究结果。根据已发表的研究结果 [13 - 14] ,TAF 阻断 HBV 母婴传播的效果和安全性良好,有望成为阻断 HBV 母婴传播的新选择。未来还需要开展更严格的随机对照研究,为 TAF 阻断 HBV 母婴传播提供更高级别的循证医学证据。 2. 无 HBIG 的母婴传播阻断方案 :感染 HBV 母亲的新生儿出生 12 h 内接种乙肝疫苗和 HBIG 是标准的阻断 HBV 母婴传播的方案,在国内外得到广泛的应用并取得了很好的阻断效果。然而,在欠发达的国家和地区,HBIG 的可及性很低,在没有 HBIG 的情况下,妊娠期抗病毒干预结合婴儿乙肝疫苗接种的阻断效果如何,是一个新的有实际意义的科学问题。国内已开展多中心的临床试验对这一问题进行研究。 3. 妊娠期服用抗病毒药物的安全性 :已发表的研究表明 [11,12,27 - 28] ,妊娠期服用抗病毒药物对胎儿的生长发育无不良影响,未增加婴儿出生缺陷的发生率,且对婴儿出生后的骨代谢和生长发育无明显影响。然而,由于阻断 HBV 母婴传播是在妊娠晚期启动抗病毒治疗,所以目前的安全性数据大多来源于妊娠晚期服用抗病毒药物的情况,而妊娠 24 周之前特别是妊娠 12 周之前服药的安全性数据很少,尤其缺乏在妊娠不同阶段抗病毒治疗的安全性比较研究。 美国于 1989 年建立了抗反转录病毒妊娠登记系统(anti - retroviral pregnancy registry, APR),目的是为了发现与妊娠期抗反转录病毒药物暴露相关的婴儿畸形。APR 是一个国际性、自愿性和前瞻性的队列研究,现已有 24 258 例妊娠期暴露于抗病毒药物孕妇的登记数据 [27] 。我国孕产妇中 HBV 感染率约为 6.3% [17] ,每年约有 100 万例感染 HBV 的孕产妇,妊娠期服用抗病毒药物的孕妇数量在不断增加。因此,有必要建立我国的妊娠期抗病毒治疗孕妇的登记系统,为基于大数据的抗病毒药物妊娠安全性研究奠定基础。 4. 母亲产后停药的随访 :已发表的相关指南(共识)均推荐为阻断 HBV 母婴传播而服用抗病毒药物的母亲产后即可停药,但在临床实践中发现有部分妊娠晚期开始抗病毒治疗的母亲,产后复查 HBV DNA 低于检测下限,且 HBsAg 和(或)HBeAg 水平显著下降,提示可能已并非处于 HBV 感染的免疫耐受期,因此继续抗病毒治疗有望取得良好效果。当前尚缺乏对感染 HBV 母亲分娩停药后长期随访的研究。建立母亲产后停药随访队列,观察病毒学、血清学和生物化学指标的变化,可以为优化产后管理提供依据。 参考文献 [1] WHO global health sector strategy on viral hepatitis 2016–2021[M]. Geneva: World Health Organization, 2016. https: //www.who.int/ hepatitis/strategy2016-2021/ghss-hep/en/ [2] 中国肝炎防治基金会 , 中华医学会肝病学分会 , 中华医学会感 染病学分会 . 乙型肝炎母婴阻断临床管理流程 [J]. 中华肝脏病 杂 志 , 2017, 25(4): 254-256. DOI: 10.3760/cma.j.issn.1007-3418. 2017.04.004. [3] Hou J, Cui F, Ding Y, et al. Management algorithm for interrupting mother-to-child transmission of hepatitis B virus[J]. Clin Gastroenterol Hepatol, 2019, 17(10): 1929-1936.e1. DOI: 10.1016/ j.cgh.2018.10.007. [4] 中华医学会感染病学分会 , 中华医学会肝病学分会 . 慢性乙型 肝炎防治指南 (2019 年版 ) [J] . 中华传染病杂志 , 2019, 37 (12): 711-736. DOI: 10.3760/cma.j.issn.1000-6680.2019.12.003. [5] 中华医学会妇产科学分会产科学组 , 中华医学会围产医学分会 . 乙型肝炎病毒母婴传播预防临床指南 (2020) [J]. 中华妇产科杂 志, 2020, 55(5): 291-299. DOI: 10.3760/cma.j.cn112141-20200213- 00101. [6] World Health Organization. Prevention of mother-to-child transmission of hepatitis B virus: guidelines on antiviral prophylaxis in pregnancy[EB/OL]//https: //www.who.int/publications/i/item/978- 92-4-000270-8. [7] 中华医学会肝病学分会 . 感染乙型肝炎病毒的育龄女性临床 管理共识 [J] . 中华肝脏病杂志 , 2018, 26 (3): 204-208. DOI: 10.3760/cma.j.issn.1007-3418.2018.03.009. [8] 中华医学会感染病学分会 , GRADE 中国中心 . 中国乙型肝炎病 毒母婴传播防治指南 (2019 年版 ) [J] . 中华传染病杂志 , 2019, 37 (7): 388-396. DOI: 10.3760/cma.j.issn.1000-6680.2019.07.002. [9] Zhang H, Pan C, Pang Q, et al. Telbivudine or lamivudine use in late pregnancy safely reduces perinatal transmission of hepatitis B virus in real-life practice[J]. Hepatology, 2014, 60 (2): 468-476. DOI: 10.1002/hep.27034. [10] Chen HL, Lee CN, Chang CH, et al. Efficacy of maternal tenofovir disoproxil fumarate in interrupting mother-to-infant transmission of hepatitis B virus[J]. Hepatology, 2015, 62(2): 375-386. DOI: 10.1002/hep.27837. [11] Pan CQ, Duan Z, Dai E, et al. Tenofovir to prevent hepatitis B transmission in mothers with high viral load[J]. N Engl J Med, 2016, 374(24): 2324-2334. DOI: 10.1056/NEJMoa1508660. [12] Jourdain G, Ngo-Giang-Huong N, Harrison L, et al. Tenofovir versus placebo to prevent perinatal transmission of hepatitis B[J]. N Engl J Med, 2018, 378(10): 911-923. DOI: 10.1056/NEJMoa1708131. [13] Zeng QL, Yu ZJ, Ji F, et al. Tenofovir alafenamide to prevent perinatal hepatitis B transmission: a multicenter, prospective, observational study[J]. Clin Infect Dis, 2021 Jan 4: ciaa1939. DOI: 10.1093/cid/ciaa1939. Epub ahead of print. [14] Ding Y, Cao L, Zhu L, et al. Efficacy and safety of tenofovir alafenamide fumarate for preventing mother to child transmission of hepatitis B virus: a national cohort study[J]. Aliment Pharmacol Ther, 2020, 52(8): 1377-1386. DOI: 10.1111/apt.16043. [15] Yin X, Han G, Zhang H, et al. A real-world prospective study of mother-to-child transmission of HBV in China using a mobile health application (shield 01)[J]. J Clin Transl Hepatol, 2020, 8(1): 1-8. DOI: 10.14218/JCTH.2019.00057. [16] Polaris Observatory Collaborators. Global prevalence, treatment, and prevention of hepatitis B virus infection in 2016: a modelling study[J]. Lancet Gastroenterol Hepatol, 2018, 3(6): 383-403. DOI: 10.1016/S2468-1253(18)30056-6. [17] Cui F, Woodring J, Chan P, et al. Considerations of antiviral treatment to interrupt mother-to-child transmission of hepatitis B virus in China[J]. Int J Epidemiol, 2018, 47(5): 1529-1537. DOI: 10.1093/ije/dyy077. [18] 国家卫生和健康委员会妇幼司 . 预防艾滋病、梅毒和乙型乙肝 肝炎母婴传播工作规范 (2020 年版 )[EB/OL]//http: //www.nhc. gov.cn/fys/s3581/202011/fc7b46b2b48b45a69bd390ae3a62d065. shtml. [19] Pan CQ, Zou HB, Chen Y, et al. Cesarean section reduces perinatal transmission of hepatitis B virus infection from hepatitis B surface antigen-positive women to their infants[J]. Clin Gastroenterol Hepatol, 2013, 11(10): 1349-1355. DOI: 10.1016/j.cgh.2013.04.026. [20] Peng S, Wan Z, Liu T, et al. Cesarean section reduces the risk of early mother-to-child transmission of hepatitis B virus[J]. Dig Liver Dis, 2018, 50(10): 1076-1080. DOI: 10.1016/j.dld.2018.05.004. [21] Chen HL, Cai JY, Song YP, et al. Vaginal delivery and HBV mother to child transmission risk after immunoprophylaxis: a systematic review and a meta-analysis[J]. Midwifery, 2019, 74: 116-125. DOI: 10.1016/j.midw.2019.03.024. [22] Schillie S, Vellozzi C, Reingold A, et al. Prevention of hepatitis B virus infection in the united states: recommendations of the advisory committee on immunization practices[J]. MMWR Recomm Rep, 2018, 67(1): 1-31. DOI: 10.15585/mmwr.rr6701a1. [23] Chen X, Chen J, Wen J, et al. Breastfeeding is not a risk factor for mother-to-child transmission of hepatitis B virus[J]. PLoS One, 2013, 8(1): e55303. DOI: 10.1371/journal.pone.0055303. [24] Shi Z, Yang Y, Wang H, et al. Breastfeeding of newborns by mothers carrying hepatitis B virus: a meta-analysis and systematic review[J]. Arch Pediatr Adolesc Med, 2011, 165(9): 837-846. DOI: 10.1001/ archpediatrics.2011.72. [25] Ehrhardt S, Xie C, Guo N, et al. Breastfeeding while taking lamivudine or tenofovir disoproxil fumarate: a review of the evidence[J]. Clin Infect Dis, 2015, 60(2): 275-278. DOI: 10.1093/ cid/ciu798. [26] Yi W, Pan CQ, Li MH, et al. The characteristics and predictors of postpartum hepatitis flares in women with chronic hepatitis B[J]. Am J Gastroenterol, 2018, 113(5): 686-693. DOI: 10.1038/s41395-018- 0010-2. [27] Antiretroviral pregnancy registry interim report for 1 January 1989- 31 January 2020[EB/OL]//http: //www.apregistry.com/forms/exec- summary.pdf. [28] Wen WH, Chen HL, Shih TT, et al. Long-term growth and bone development in children of HBV-infected mothers with and without fetal exposure to tenofovir disoproxil fumarate [J]. J Hepatol, 2020, 72(6): 1082-1087. DOI: 10.1016/j.jhep.2020.01.021.
 康文 副主任医师 空军军医大学唐都医院 传染病科7494人已读
康文 副主任医师 空军军医大学唐都医院 传染病科7494人已读 - 学术前沿 美国更新艾滋病药物预防(PrEP&PEP)建议(2020)
转载自i卫士:https://mp.weixin.qq.com/s/4XISu617owBS_6zUXftr3g 美国国际抗病毒学会(IAS-USA)发布2020年指南更新了关于艾滋病药物预防(PrEP&PEP)的主要建议。相关结果于2020年10月14日发表在JAMA期刊上,标题为“Antiretroviral Drugs for Treatment and Prevention of HIV Infection in Adults---2020 Recommendations of the International Antiviral Society–USA Panel”。美国阿拉巴马大学伯明翰分校的Michael S. Saag医学博士及其同事们收集了549份引文,作为2018年IAS-USA建议以来的新证据进行指南的更新,其中关于HIV药物预防给出如下建议。 关于HIV暴露前预防(PrEP) 适用人群:PrEP推荐用于存在HIV感染风险的个体。如用于但不局限于MSM,双性性行为者,不使用安全套者;变性者;来自HIV新发感染大于等于3%地区的或性伴来自这些地区的人;提供商业性行为的人;多性伴的人;性病感染的人;曾经被监禁过的人群或其性伴被监禁过的人;注射吸毒者。 用药:针对选择使用PrEP的个体建议尽早启动用药;TDF/FTC一天一次。 对于MSM,PrEP第一天建议服用两剂次;有肾功能障碍问题或存在肾功能障碍风险的MSM,骨质减少或骨质疏松症者推荐使用 TAF/FTC一天一次;2-1-1口服药物预防方案推荐仅用于MSM人群;每8周注射一次的cabotegravir被推荐用于与男性发生性行为的顺性别和变性人 (等待有关管理机构批准和药物准备) 。 口服用药PrEP监测 启动前 HIV抗体抗原检测(怀疑急性期病人做HIV RNA检测);血肌酐水平检测;HBV表面抗原检测;HCV IgG抗体(知晓既往感染HCV,需检测HCV核酸结果);MSM和注射吸毒者需进行甲肝抗体检测;生殖道和非生殖道淋病、砂眼衣原体核酸扩增检测(NAAT);梅毒检测。 用药中 第一月:HIV抗体抗原检测 每季度:HIV抗体抗原检测;估计的肌酐清除率(第一季度检测,之后每年一次,每3-6个月评估病人是否存在肾脏损伤或存在肾脏损伤的风险);生殖道和非生殖道淋病、砂眼衣原体核酸扩增检测(NAAT);梅毒检测;孕检(潜在生育人群)。 每年:HIV抗体抗原检测;估计的肌酐清除率;HCV IgG抗体(如果肝功结果异常时,注射吸毒者或使用助性药物的MSM每3-6个月检测一次)。 其他建议:连续停止用药7天或以上的人重启用药建议重新做HIV抗体抗原检测;对于怀疑使用PrEP依从性差、有高危暴露、PrEP中断和连续使用28天3联PEP阻断的人群推荐重新做HIV抗体抗原检测;变性人由于使用外源性雌激素或雄激素阻断剂导致替诺福韦/替诺福韦代谢物浓度减少30%,从而可能降低保护作用,推荐使用应用支持每日服药最大程度依从性的其他措施 关于HIV暴露后预防(PEP) HIV暴露后预防用药方案推荐3药ART,最好在暴露后24小时之内用药,最晚不超过72小时,连续用药28天。 如果在接受PrEP期间感染了HIV,建议开始先采用过渡治疗方案 DTG-,BIC- 或者DRV/r,根据临床耐药实验结果该方案可以进行调整。
 康文 副主任医师 空军军医大学唐都医院 传染病科8015人已读
康文 副主任医师 空军军医大学唐都医院 传染病科8015人已读 - 就诊指南 招募HIV合并慢性丙型感染患者(2019年7月)
患者朋友: 目前空军军医大学唐都医院感染科正在进行“十三五”国家科技重大专项课题《HIV合并HCV感染人群抗病毒治疗研究》,这是一项治疗HIV感染合并慢性丙型肝炎的临床研究,该研究预计在全国5家医院(包括本院)招募300例患者,其中本院预计有20例患者入组。若您符合以下条件且愿意参与研究,请我们联系。成功入组后将给您免费提供丙肝口服治疗药物(既往治愈率98%以上),以及16周的1天1片的艾滋病治疗药物(非国免药)。入组条件如下: 1、年龄18-65岁; 2、同时感染HIV和丙型肝炎病毒者 3、HIV确诊超过6个月,如已经接受治疗的HIV感染者,最近1年内HIV RNA需低于检测下限; 4、抗HCV或HCV RNA阳性超过6个月,未使用过小分子药物治疗丙肝;或曾经使用过干扰素治疗丙肝,治疗失败者; 5、近3月内没有发生机会性感染或肿瘤; 6、没有肝硬化; 7、没有吸毒和酗酒; 8、自愿签署患者知情同意书,并能保证接受随访 如对本研究感兴趣或想了解更多的信息,请与下列人员联系: 研究医师:康文 电话号码:029-84777762
康文 副主任医师 空军军医大学唐都医院 传染病科1914人已读 - 医学科普 担心感染艾滋病?后悔药了解一下(转载自“感染科王医生”微信公众号)
一时冲动,做了不该做的事,事后对方竟然说自己感染了HIV,已经确诊了,怎么办? 给患者拔针的时候不小心被针头刺破了皮肤,患者是个HIV感染者,怎么办? 别恐慌,虽然时光不能倒流,但在这个世界上,
 康文 副主任医师 空军军医大学唐都医院 传染病科6672人已读
康文 副主任医师 空军军医大学唐都医院 传染病科6672人已读





